Авторы: Фомин А. А., Новиков Ю. В., Першаков Д. Р., Фомин М. А.
Введение
Лечение гнойно-некротических поражений нижних конечностей является одной из актуальных проблем хирургии, диабетологии и флебологии. Если нарушение обменных процессов можно нормализовать проведением соответствующей консервативной терапии, то анатомические изменения можно исправить только оперативным путем. Довольно долго методом выбора лечения длительно незаживающих ран и язв считалось ранняя, свободная аутодермопластика. Однако нередко подобная тактика не приносила успеха из-за отторжения или некроза кожного лоскута. Неудачи кожно-пластических вмешательств могут быть обусловлены многочисленными причинами, главными из которых считают недостаточную подготовку воспринимающего ложа, снижение репаративных возможностей организма, в том числе и из-за диабета и пожилого возраста больных. Весьма существенную роль играет и состояние микроциркуляции в пораженной конечности, без улучшения которой невозможно рассчитывать на положительный результат. В научных хирургических публикациях последних лет большое внимание уделяется проблеме лечению гнойно-некротических осложнений синдрома диабетической стопы. В связи с этим рассматриваются вопросы восстановления региональной гемодинамики, сроки и объем оперативных вмешательств. Одним из методов ликвидации раневых дефектов нижних конечностей у больных является аутодермопластика расщепленным кожным лоскутом.
Остаются до конца нерешенными вопросы о сроках проведения аутодермопластики, обоснованности и длительности проведения предоперационной подготовки, улучшение региональной гемодинамики, подготовки к аутодермопластике воспринимающего ложа и донорского участка кожи.
С 2006 года накоплен большой материал по данной проблеме, который обобщен в статье.
Цель исследования
Улучшить результаты лечения гнойных ран при трофических нарушениях нижних конечностей (сахарный диабет, хроническая венозная недостаточность, хроническая артериальная недостаточность) путем совершенствования приемов аутодермопластики и оценке уровня микорциркуляции раневого ложа.
Материал и методы
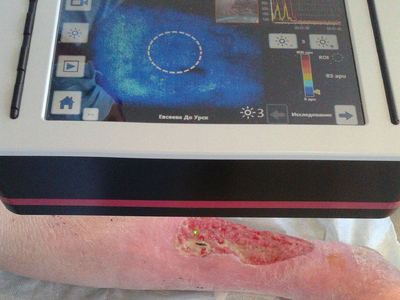
В основу работы положен анализ лечения гигантских (более 50 см²) трофических язв нижних конечностей при сахарном диабете (27 пациентов), хронической венозной (32 больных) и артериальной (24 человека) недостаточности период с 2009 по 2013 год. Группу сравнения составили 60 больных сопоставимые по возрасту, виду патологии и сопутствующей патологии лечившихся традиционными способами. Средний возраст оставил 69±3,7 лет. Микроциркуляцию язвенной поверхности измеряли с помощью аппарата Easy-LDI (Швейцария). Предоперационною подготовку раневого ложа производили с помощью вакуум-терапии, ультразвуковой кавитации и адресной лимфотропной антибиотикотерапии. Забор аутокожи осуществляли дисковымдерматомом с последующей перфорацией лоскутов. Изучение микроциркуляции раневоговоспринимаюшего ложа у наших пациентов осуществляли с помощью метода лазерной допплеровской визуализации на аппарате LDI фирмы AIMAGO (Швейцария). Технология LDI (LaserDopplerImaging), в русскоязычной литературе — лазерная допплеровская визуализация, позволяет проводить бесконтактное наблюдение за микрокровотоком на площади 100 см², с глубиной зондируемого слоя до 2 мм, одномоментной видеозаписью исследования и возможностью измерений сразу в нескольких близлежащих точках. При этом технически исследование настолько просто, что может быть выполнено средним медперсоналом, поскольку воспроизводимость практически не зависит от квалификации исследователя. Анализ полученного изображения производился в режиме реального времени.
Полученные данные заносились в память прибора, что позволяло при необходимости повторно просмотреть видеозапись измерения. Учитывали число относительных перфузионных единиц (apu), отражающих количество крови протекающей в единицу времени в одной кубической единице объема ткани. Вакуумировнаие язвенного дефекта осуществляли по предложенной методике. Суть ее заключается в том, что вместо традиционной губки используются обычные подгузники. Их прекрасная гигроскопичность не уступает таковым у поролона, и втоже время они более привлекательны по цене, бесплатны для больных в стационарах, выпускаются в достаточном количестве нашей промышленностью. Форма подгузника позволяет накладывать его так, что абсорбционная поверхность полностью закрывает кожные покровы и не мацерирует их.
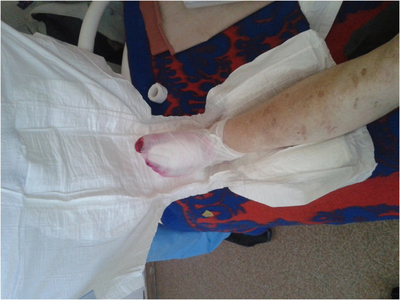
Методика применения подгузника для вакуум-терапии заключается в следующем. На раневую поверхность накладывается стерильная марлевая повязка. Поверх ее укладывается подгузник (рис. 2). Причем последний накладывается целиком, гигроскопичной поверхностью к коже, предупреждая опрелость и ее мацерацию.
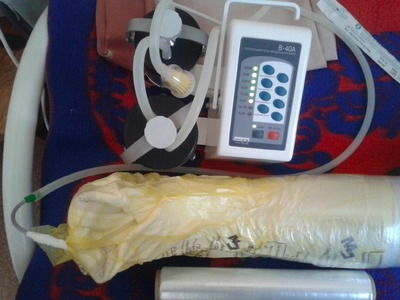
Между подгузником и стерильной повязкой помещается силиконовый катетер Нелатона № 14 по подошвенной части стопы с переходом на заднюю часть нижней трети голени. Такая укладка улучшает отток раневого отделяемого в горизонтальном положении больного. Поверх подгузника одевается мешок для сбора медицинских отходов. В верхней трети голени он фиксируется к кожным покровам клеящейся медицинской пленкой. Свободный конец катетера Нелатона выводится через прокол в нижнем углу пакета, герметизируется и подсоединяется к отсосу (рис. 3).
Перфорационное отверстие в пакете герметизируется лейкопластырем. Сравнительный анализ использования поролона и подгузника проведен в группах больных с гнойными ранами в фазу выраженной экссудации у больных сахарным диабетом. По всем параметрам предпочтительнее оказалось применение подгузника. Обладая одинаковой всасывательной способностью, под ним не преют и не мацерируются кожные покровы, себестоимость подгузника в 2 раза дешевле, чем поролона. Эти обстоятельства побудили нас в методике использования вакуум-терапии применять подгузники. Эффективность вакуум-терапии гнойной раны оценивали с помощью показателей микроциркуляции (лазерная допплеровская визуализация — LDI) и регистрации отека тканей измерением диаметра голени в средней трети. Результаты исследования представлены в табл. 1.
Таблица 1. Изменение показателей микроциркуляции и уменьшение отека гнойной раны под влиянием вакуум-терапии
| Параметры измерения | До вакуум-терапии | После вакуум-терапии | р |
|---|---|---|---|
| Показатели микроциркуляции | 4,7±2,5 apu | 10,3±1,7 apu | р ≤ 0,05 |
| Окружность голени в средней трети | 32,4±2,7 см | 27,1±1,4 см | р ≤ 0,05 |
Из таблицы следует, что вакуум-терапия улучшает микроциркуляцию пораженных тканей на 54,4 % и уменьшает на 25,7 % отек тканей за счет удаления межклеточной жидкости. Это помогает раннему очищению и развитию грануляционной ткани, что в конечном итоге ускоряет заживление раны.
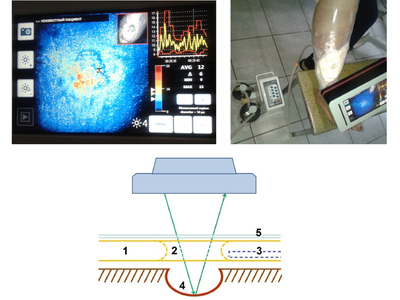
Пониженное атмосферное давление усиливает приток крови к зоне вакуума, тем самым усиливается фагоцитоз, рана быстрее очищается и заживает. Однако, при микроангиопатиях как атеросклеротического так и диабетического генеза проницаемость капиллярного русла страдает. Поэтому очень важно оценить степень разрежения для улучшения микроциркуляции и регулировать ее в динамике в режиме реального времени. При выполнении стандартного метода оценить это не представляется возможным, так как раневая поверхность закрыта повязкой. Предлагаем способ «управляемой микроциркуляции» (рис. 4) в ране при вакуум–терапии в режиме реального времени. Для этого в подгузнике (1) выкраиваем окно (2), между подгузником и повязкой (4) вставляем дренажную трубку (3), отводящую воздух, всю конструкцию изолируем пленочным материалом (5). Через сформированное окно допплеровским дистанционным флоуметром LDI (Швейцария) выполняем функционально-метаболическую визуализацию (сочетая визуализацию микроциркуляторного русла со стимуляцией пациента — изменение температурного режима, применения вазоактивных проб, лекарственные нагрузки, кислородные пробы и т. д.)
Исследование проведено на 30 пациентах (мужчин — 16, женщин — 14 ). Средний возраст — 64±12,5 лет. Микроангиопатия атеросклеротического генеза — у 10 больных, диабетическая — у 10 пациентов, флебологическая — у 10.
Динамическое наблюдение за параметрами микроциркуляции позволяет своевременно выполнить ее коррекцию путем подбора режима отрицательного давления, применения медикаментозной терапии и т. д. Проведенное исследование показало, что пленочное покрытие при прохождении лазерного пучка не искажает результаты исследования микроциркуляции.
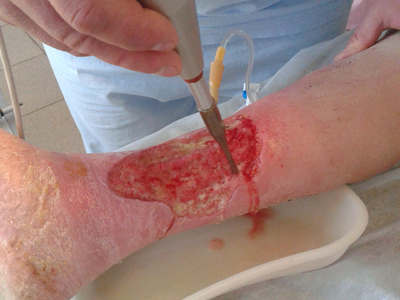
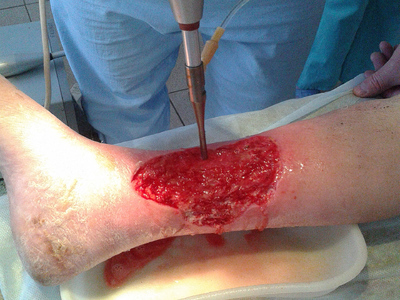
Непосредственно перед наложением перфорированного аутодермального лоскута воспринимающее ложе обрабатывали антисептиком с учетом чувствительности флоры раневой поверхности с помощью ультразвуковой кавитации (рис. 5, 6).
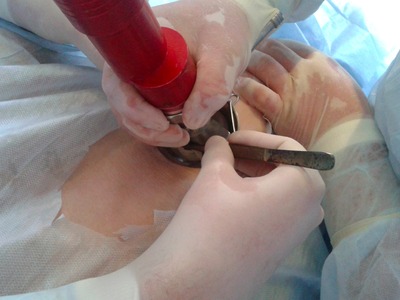
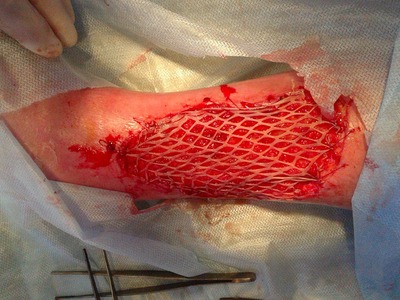
Затем дисковым дерматомом под местной анестезией раствором новокаина 0,5 % (80,0) выполняли забор аутокожи (рис. 7), перфорировали его (рис. 8) и пересаживали на гранулирующую ткань язвенной поверхности (рис. 9)
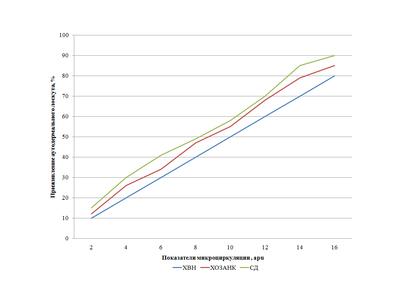
В доступной нам литературе мы не нашли показаний к дермопластике с учетом микроциркуляции грануляций. Поэтому изучили влияние микроциркуляции грануляционной ткани в язвенной поверхности у больных с сахарным диабетом, хронической венозной недостаточностью и хронической ишемией конечности на приживаемость кожного аутотранстплантата. Полученные данные представлены на рис. 10 (по вертикали — показатели приживления аутодермального лоскута, выраженный в %, по горизонтали — показатели микроциркуляции, представленные в apu).
Из рисунка видно, что с увеличением показателей микроциркуляции возрастает доля приживляемости аутотрансплантата, причем у больных сахарным диабетом она несколько замедлена, по-видимому, это связано с более выраженным поражением микроциркуляторного русла при данной патологии. Оптимальными показателями микроциркуляции грануляционной ткани гарантирующими прижевление аутокожи явились значения от 14,3±1,17 apu до 16,5±1,5 apu.
Самостоятельное закрытие гигантских трофических дефектов нижних конечностей весьма проблематично и обычно заканчивается грубым келлоидом, уродующим ногу и нарушающим функцию нижних конечностей. Применение аутодермопластики значительно облегчает эту задачу. Применение нашей методики данного оперативного пособия в лечении грубых дефектов нижних конечностей показало значительное преимущество перед традиционными методами (табл. 2).
Таблица 2. Показатели приживления аутокожи при закрытии язвенных дефектов при гигантских трофических язвах в основной и контрольной группах, %
| Заболевание | Основная группа | Контрольная группа |
|---|---|---|
| Сахарный диабет n-20 | 93±3,7* | 54±8,3* |
| ХОЗАНКn-10 | 87±4,1* | 67±4,8* |
| ХВНn-10 | 80,1±2,8* | 71±3,2* |
Список литературы
- Глухов А. А., Аралова М. В. Эпидемиология венозных трофических язв. 2-й международный конгресс, посвященный 70-летию Института хирургии им. А. В. Вишневского. «Раны и раневая инфекция». с. 113–114.
- Давыдов Ю. А., Ларичев А. Б. Вакуум-терапия и раневой процесс. Ярославль. 1995.
- Дуванский В. А., Мараеав В. В. Лазерная допплеровская флоуметрия как метод оценки микроциркуляции ран. II международный конгресс, посвященный 70-летию Института хирургии им. А. В. Вишневского. «Раныи раневая инфекция», c. 130–131.
- Ларичев А. Б., Антонюк А. В., Кузьмин В. С. Вакуум терапия в лечении хронических ран. Ярославль. 2007.